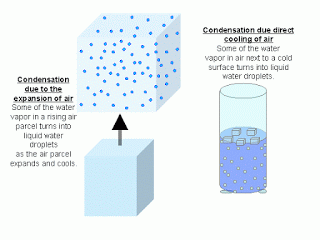
A. Pengertian Koloid
Dalam kehidupan sehari-hari ini, sering kita temui beberapa
produk yang merupakan campuran dari beberapa zat, tetapi zat tersebut dapat
bercampur secara merata/ homogen. Misalnya serbuk susu bercampur merata dengan
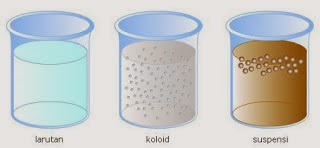
air panas. Sistem tersebut merupakan sistem koloid. Koloid adalah suatu
campuran zat heterogen (dua fase) antara dua zat atau lebih di mana
partikel-partikel zat yang berukuran koloid tersebar/terdispersi secara merata
di dalam zat lain. Zat yang tersebar atau terdispersi sebagai partikel koloid disebut
fase terdispersi. Sedangkan zat yang merupakan fase kontinu dimana partikel
koloid terdispersi disebut medium pendispersi. Ukuran partikel koloid berkisar
antara 10-7sampai dengan 10-4 cm. Ukuran yang
dimaksud dapat berupa diameter, panjang, lebar, maupun tebal dari suatu
partikel. Partikel dapat terdiri atas atom, molekul kecil atau molekulyang
sangat besar. Koloid emas terdiri atas partikel-partikel dengan bebagai ukuran,
yang masing-masing mengandung jutaan atom emas atau lebih. Koloid belerang terdiri
atas partikel-partikel yangmengandung sekitar seribu molekul S8. Suatu contoh
molekul yang sangat besar (disebut juga molekul makro) ialah haemoglobin. Berat
molekul dari molekul ini 66800 s.m.a dan mempunyai diametersekitar 6 x 10-7.
B. Jenis-jenis Koloid
No.
|
Fase Terdispersi
|
Fase Pendispersi
|
Nama
|
Contoh
|
1.
|
Padat
|
Gas
|
Aerosol
|
Asap (smoke), debu di udara
|
2.
|
Padat
|
Cair
|
Sol
|
Sol emas, sol belerang, tinta, cat
|
3.
|
Padat
|
Padat
|
Sol padat
|
Gelas berwarna, intan hitam
|
4.
|
Cair
|
Gas
|
Aerosol
|
Kabut (fog) dan awan
|
5.
|
Cair
|
Cair
|
Emulsi
|
Susu, minyak ikan
|
6.
|
Cair
|
Padat
|
Emulsi padat
|
Jeli, mutiara
|
7.
|
Gas
|
Cair
|
Buih
|
Buih sabun
|
8.
|
Gas
|
Padat
|
Buih padat
|
Karet busa, batu apung, stirofoam
|
a. Sol
Merupakan sistem koloid dengan fase terdispersi berupa zat
padat dalam medium pendispersi zat cair. Contohnya sol sabun, sol
deterjen, sol kanji.
b. Aerosol
Merupakan sistem koloid dengan fase terdispersi padat atau
cair dalam medium pendispersi gas.Contoh produk yang dibuat dalam bentuk
aerosol, hairspray, semprot obat nyamuk, farfum, cat semprot. Untuk
menghasilkan aerosol diperlukan suatu bahan pendorong(propelan aerosol). Bahan
pendorong yang banyak digunakan adalah CFC dan karbon dioksida.
c. Emulsi
Merupakan sistem koloid
dengan fase terdispersi cair dalam medium pendispersi cair. Syarat
terjadinya emulsi adalah kedua jenis zat cair tersebut tidak saling
melarutkan.Emulsi digolongkan ke dalam dua bagian yaitu :
- Emulsi
minyak dalam air ( M/A )
Contoh : santan, susu, lateks
- Emulsi
air dalam minyak ( A/M )
Contoh : mayonaise, minyak
bumi, minyak ikan
Untuk membuat emulsi diperlukan zat pengemulsi (emulgator).
Contohnya, sabun mengemulsikan minyak ke dalam air, kasein dalam susu,
kuning telur dalam mayonaise.
d. Buih
Merupakan sistem koloid dengan fase terdispersi gas
dalam medium pendispersi cair. Seperti halnya emulsi untuk menstabilkan buih
diperlukan zat pembuih, misalnya sabun, deterjen, protein. Buih digunakan pada
proses pengolahan biji logam, pada alat pemadam kebakaran.Adakalanya buih tidak
dikehendaki, untuk memecah/mencegah buih dapat digunakan zat eter, isoamil
alkohol.
e. Gel
Merupakan koloid yang setengah kaku ( antara padat dan
cair).Contohnya agar-agar, lem kanji, selai, gelatin, gel silika. Gel dapat
terbentuk dari sol yang zat terdispersinya mengadsorpsi medium pendispersinya.
C. Sifat-sifat Koloid
Beberapa sifat-sifat koloid yang khas, yaitu:
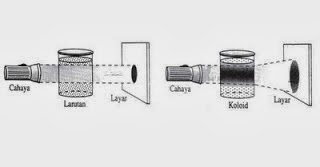
1. Efek Tyndall
Efek Tyndall adalah suatu efek penghamburan berkas sinar
oleh partikel-partikel yang terdapat dalam sistem koloid, sehingga jalannya
berkas sinar terlihat. Efek tyndall ini dapat digunakan untuk membedakan sistem
koloid dari larutan.
2. Gerak Brown
Gerak Brown adalah gerakan terpatah-terpatah (gerak zig-zag)
yang terus-menerus dalam sistem koloid. Adanya gerak brown membuat
partikel-partikel koloid dapat mengatasi pengaruh gravitasi sehingga
partikel-partikel ini tidak memisahkan diri dari medium pendispersinya.
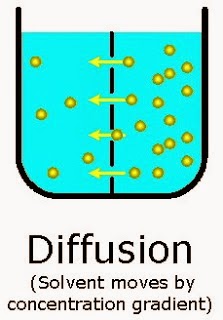
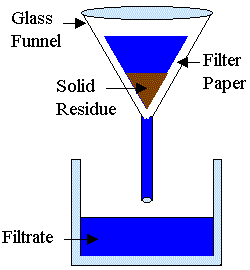
3. Difusi dan Filtrasi
Partikel koloid lebih sulit berdifusi bila dibandingkan
dengan larutan sejati. Hal ini disebabkan ukuran partikel koloid lebih besar
dibandingkan dengan partikel larutan sejati. Selain itu ukuran partikel koloid
juga menyebabkan partikel koloid tidak dapat disaring dengan kertas biasa,
tetapi harus dengan penyaring ultra.
4. Adsorpsi
Adsorpsi adalah proses penyerapan zat atau partikel atau
molekul pada permukaan diri zat tersebut sehingga koloid akan memiliki muatan
listrik. Antara partikel koloid dengan ion-ion yang diadsorpsi akan membentuk
beberapa lapisan, yaitu:
a) Lapisan pertama ialah lapisan inti
yang bersifat netral, terdiri atas partikel koloid netral.
b) Lapisan ion dalam ialah lapisan ion-ion
yang diadsorpsi oleh koloid.
c) Lapisan ion luar.
d) Kesetabilan koloid.
5. Koagulasi
Partikel-partikel koloid bersifat stabil karena memiliki
muatan listrik yang sejenis. Apabila muatan listrik tersebut hilang, maka
partikel-partikel koloid akan bergabung membentuk gumpalan. Proses penggumpalan
ini disebut flokulasi(flocculation) dan gumpalannya disebut flok(flocculant).
Gumpalan ini akan mengendap akibat pengaruh gravitasi. Proses penggumpalan
partikel-partikel koloid dan pengendapannya ini disebut koagulasi. Penghilangan
muatan listrik pada partikel koloid ini dapat dilakukan dengan empat cara,
yaitu:
a) Elektroforesis
Elektroforesis adalah peristiwa pemisahan koloid yang
bermuatan. Partikel-partikel koloid yang bermuatan dengan bantuan arus listrik
akan mengalir ke masing-masing elektroda yang bermuatannya berlawanan. Partikel
yang bermuatan positif bergerak menuju elektroda negatif, begitupun sebaliknya.
Menyebabkan partikel-partikel tersebut akan kehilangan muatannya, sehingga
menggumpal dan mengendap di elektrode.
b) Penambahan koloid lain dengan muatan
berlawanan
Apabila suatu sistem koloid ditambahkan koloid lain dengan
muatan berlawanan, maka kedua sistem koloid tersebut akan saling mengadsorpsi
dan menjadi netral. Akibatnya terbentuk koagulasi.
c) Penambahan elektrolit
Jika suatu elektrolit ditambahkan ke dalam sistem koloid,
maka partikel-partikel koloid yang bermuatan negatif akan menarik ion positif
(kation) dari elektrolit. Sementara itu, partikel-partikel yang bermuatan
positif akan menarik ion negatif(anion) dari elektrolit. Hal ini menyebabkan
partikel-partikel koloid tersebut dikelilingi oleh lapisan kedua yang memiliki
muatan berlawanan dengan muatan lapisan pertama. Apabila jarak antara lapisan
pertama dan kedua cukup dekat, maka muatan keduanya akan hilang sehingga
terjadi koagulasi.
d) Pendidihan
Kenaikan suhu sistem koloid menyebabkan jumlah tumbukan
antara partikel-partikel sol dengan molekul-molekul air menjadi bertambah
banyak. Yang akan menyebabkan lepasnya elektrolit yang teradsorpsi
pada permukaan partikel koloid. Akibatnya partikel-partikel koloid menjadi
tidak bermuatan sehingga terjadi koagulasi.
6. Koloid Pelindung
Koloid pelindung adalah koloid yang dapat melindungi koloid
dari proses koagulasi atau penggumpalan. Ada beberapa koloid pelindung yang
digunakan pada emulsi, misalnya casein dalam susu. Jenis koloid ini disebut
emuglatol.
7. Koloid Liofil dan koloid
Liofob
Umumnya terjadi pada koloid yang fase terdispersinya padatan
dan mediumnya cairan atau berupa sol, sehingga lebih dikenal sebagai sol liofil
atau sol liofob.
Sol liofil adalah sol di mana fase terdispersinya senang
akan medium pendispersinya (senang akan cairan) atau di katakan juga afinitas
atau daya tarik terhadap mediumnya sangat kuat.
Sol liofob adalah kebalikan dari sol liofil, di mana
partikel fase terdispersinya kurang atau tidak senang akan cairannya
(mediumnya).
D. Pembuatan Koloid Sol
1. Metode Kondensasi
Metode dimana partikel-partikel kecil larutan bergabung
membentuk partikel-partikel berukuran koloid. Hal ini dilakukan dengan reaksi
kimia(dekomposisi rangkap, hidrolisis, dan redoks) atau penggantian pelarut.
a) Dekomposisi
rangkap
Sol AS2S3 dibuat dengan
mengalirkan gas H2S perlahan melalui larutan AS2O3 dingin
sampai terbentuk sol AS2S3 yang berwarna kuning
terang
AS2O3(aq) +3H2S(g) à AS2S3(koloid)
+ 3H2O(l)
b) Reaksi
hidrolisis
Sol Al(OH)3 dapat diperoleh dari reaksi
hidrolisis garam Fe dalam air mendidih.
AlCl3(aq) + 3H2O(l) à Al(OH)3(koloid)
+3HCl(aq)
c) Reaksi Redoks
Sol belerang dapat dibuat dengan mengalirkan gas H2S
ke dalam larutan SO2
2H2S(g) + SO2(aq)à 3S(koloid) +2H2O
d) Penggantian Pelarut
Belerang sukar larut dalam air tetapi mudah larut dalam
alkohol. Jadi, untuk membuat sol belerang dengan pendispersi air, belerang
dilarutkan dahulu dalam etanol sampai jenuh. Setelah itu, larutan belerang
dalam dalam etanol ditambahkan sedikit demi sedikit ke dalam air sambil
diaduk.Belerang akan menggumpal menjadi partikel-partikel koloid akibat
penurunan kelarutan belerang dalam air.
2. Metode Dispersi
Metode dimana partikel-partikel besar dipecah menjadi
partikel-partikel berukuran koloid. Ada tiga metode yang digunakan, yakni :
a) Cara mekanik
Pengahalusan partikel-partikel kasar zat padat dengan
penggilingan untuk membentuk partikel-partikel berukuran koloid. Alat yang
digunakan disebut penggilingan koloid.
b) Cara peptisasi
Cara peptisasi adalah proses dispersi endapan menjadi sistem
koloid dengan perubahan zat pemecah. Zat pemecah dapat berupa elektrolit
khususnya ion sejenis ataupun pelarut tertentu.
c) Cara busur Bredig
Cara busur bredig digunakan untuk menbuat sol logam seperti
Ag, Au, Pt.
Di dalam pembuatan suatu sistem koloid sering terdapat
partikel-partikel zat terlarut yang tidak diinginkan. Partikel-partikel ini
dapat mengganggu kestabilan koloid sehingga harus dihilangkan/dimurnikan. Ada
beberapa cara yang dapat digunakan, yaitu:
1. Dialisis
Dialisis adalah proses penyaringan koloid dengan menggunakan
kertas perkamen atau membran yang diletakan di dalam air yang mengalir.
2. Elektrodialisis
Proses dialisis di bawah pengaruh medan listrik.
Elektrodialisis hanya dapat digunakan untuk memisahkan partikel-partikel zat
terlarut elektrolit.
3. Penyaring ultra
Penyaring ultra dapat dibuat dari kertas yang telah diresapi
selulosa seperti selofan (cellophane).
4. Penggunaan Koloid
Dari contoh-contoh koloid yang telah disebutkan, kita dapat
melihat kecenderungan industri membuat produknya dalam bentuk koloid. Misalnya,
industri kosmetik, industri makanan, industri farmasi, dan lain-lain. Koloid
merupakan satu-satunya cara untuk menyajikan suatu campuran dari zat-zat yang
tidak saling melarutkan secara "homogen" dan stabil (pada tingkat
mikroskopis). Cat, sebagai contoh, mengandung pigmen yang tidak larut dalam air
atau medium cat, tetapi dengan sistem koloid dapat dibuat suatu campuran yang
"homogen" (merata) dan stabil. dalam kehidupan sehari-hari banyak
kegunaan koloid baik langsung maupun tidak langsung. Beberapa kegunaan koloid
adalah sebagai berikut:
1. Industri kosmetika
Bahan kosmetika seperti foundation, finishing cream dan
deodorant berbentuk koloid dan umumnya sebagai emulsi.
2. Industri tekstil
Pada proses pencelupan bahan (untuk pewarnaan) yang kurang
baik daya serapnya terhadap zat warna dapat menggunakan zat warna koloid karena
memiliki daya serap yang tinggi sehingga melekat pada tekstil.
3. Industri sabun dan
deterjen
Sabun dan deterjen merupakan emulgator untuk membentuk
emulsi antara kotoran (minyak) dengan air.
4. Kelestarian lingkungan
Untuk mengurangi polusi udara yang disebabkan oleh
pabrik-pabrik, digunakan suatu alat yang disebut cotrell. Alat ini berfungsi
untuk menyerap partikel-partikel koloid yang terdapat dalam gas buangan yang
keluar dari cerobong asap pabrik.